对于过敏性病症, 如哮喘及荨麻疹, 目前在临床上仍大多以抗组织胺剂、支气管扩张剂、白三烯拮抗剂及皮质类固醇等小分子药物为主要治疗手段, 然而这些抗过敏药物仅能达到症状缓解的作用且治疗效果有限, 对于中重度过敏病患则须长期依赖高剂量皮质类固醇来减轻症状, 伴随长期使用可能会造成免疫系统方面损害的严重副作用。因此, 近年来国际药厂朝向研发安全性高且疗效佳的治疗性抗体药物来治疗相关过敏性病症, 特别是中重度过敏患者。本公司创新药项目UB-221项目UB-221为一款可针对减少病患体内IgE浓度来控制过敏症状, 可用于治疗中重度过敏性病症的治疗性单株抗体药物, 目前正在国内开展适用于相关于治疗自发性慢性荨麻疹中重度患者的临床二期试验。
UB-221藉由以下三种路径: 游离IgE结合, B淋巴细胞 (B cell)表面的IgE结合以及与B淋巴细胞表面的CD23受体上的IgG, 藉由中和反应及抑制IgE合成降低病患体内的IgE含量来达到抑制荨麻疹或哮喘等过敏病症 (图一)。
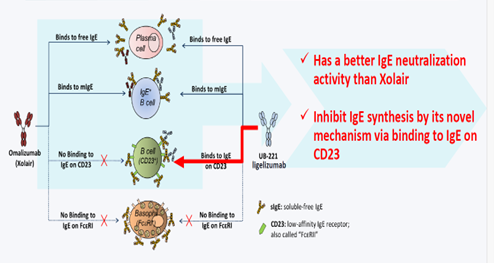
图一
在前期研究及临床试验中, UB-221以omalizumab及 ligelizumab两种目前治疗过敏中具代表性的抗IgE治疗性单抗药物作为试验的参考药物。Omalizumab是诺华(Novartis)及罗氏(Roche)公司研发的全球首款获批用于治疗重度气喘的抗IgE单抗药物, 目前在包括中国在内的96个国家地区获批使用的指标性药物; ligelizumab是诺华公司所研发新一代的抗IgE抗体药物, 藉由阻断IgE/Fcε受体1 (FcεR 1)信号通路达到治疗慢性自发性荨麻疹及重度哮喘等过敏性疾病, 其在多项临床试验中显示出比omalizumab更好的缓解荨麻疹效果且未出险显著安全性问题。根据相关试验结果, UB-221与同类型产品相比具有相当或更高的人类IgE亲和性 (图二), 更有效地与CD23受体-IgE复合体结合 (图三)以及与IgE所形成的复合体更有效地与CD23受体结合 (图四), 并且有效地抑制IgE合成 (图五)。
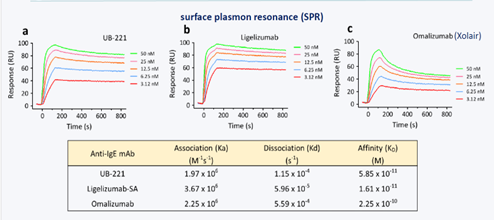
图二
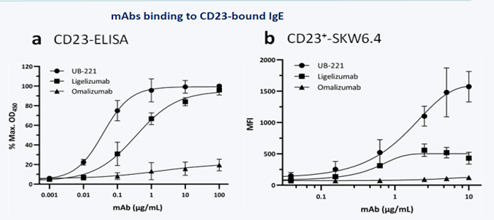
图三
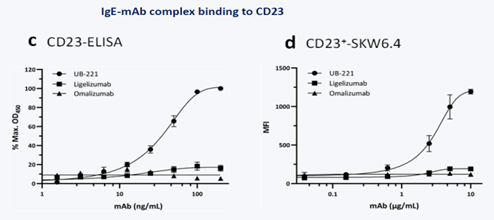
图四
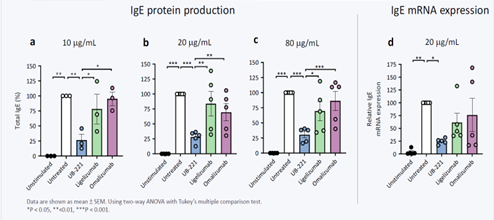
图五
根据临床一期数据发表成果 (IgE neutralizing UB-221 mAb, distinct from omalizumab and ligelizumab, exhibits CD23-mediated IgE downregulation and relieves urticaria symptoms, JCI http://jci.me/157765/pdf), 试验结果显示当UB-221与参考药 (ligelizumab)相当剂量后四周时, UB-221的complete hive response rate (HAS7= 0)的完成率为100%, 而参考药仅为40%; 当UB-221的剂量介于352到657毫克时, 受试者的hive symptoms 可维持超过3个月 (14周) (图六)。一期临床试验总结临床试验病患总数的60%达到有效控制或治疗完成的程度 (HAS7 ≤6)及80%达到有效控制的程度 (HAS7 ≤3)显示UB-221具有高度安全性及显著的治疗效果。
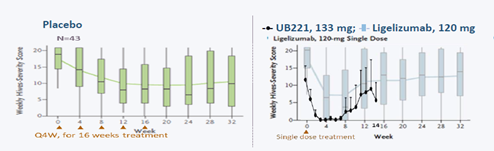
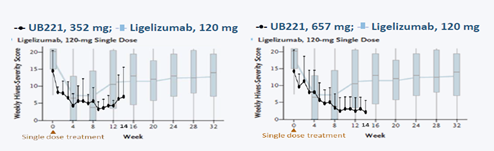
图六
综合以上相关实验结果, 以下几点来UB-221对比两款参考药的差异:
作用机制: 参照图一, 三者皆可藉由与体内游离及B淋巴细胞表面的IgE结合降低及治疗IgE诱发的过敏反应; ligelizumab 另外可以藉由阻断阻断IgE/Fcε受体1 (FcεR 1)信号通路来达到降低及治疗过敏反应; 而UB-221及ligelizumab则另外藉由与B淋巴细胞上的CD23 受体与IgE复合体结合抑制IgE合成 (ligelizumab较弱)。就作用机制对于降低病患体内IgE诱发过敏性反应, UB-221除藉中和游离IgE及阻断B淋巴细胞表面IgE诱发以外, 藉由抑制IgE合成从根本上降低IgE及其诱发的过敏反应。
前期研究结果: 参照图二, UB-221与ligelimab对游离IgE显示相当的亲和性, 皆高于omalizumab 约4倍; 参照图三, UB-221对于CD 23受体与IgE复合体的结合力明显高于omalizumab及ligelizumab (ligelizumab显示有弱的结合力); 参照图四, UB-221对于CD 23受体具有显著结合力, 而omalizumab及ligelizumab则无结合力。综合以上, UB-221及ligelizumab对于游离IgE的亲和力皆高于omalizumab表示前二者药物用于降低IgE引发的过敏性反应有更快速及更持续性的效果; 另外, UB-221对CD 23受体及CD 23受体与IgE复合体的结合性明显高于参考药显示其对于降低IgE生成的效果显至优于参考药, 参考图五显示UB-221在较低剂量条件时即可达到有效抑制IgE合成且抑制效果优于参考药。
临床试验一期结果: 根据适应症为慢性自发性荨麻疹的临床试验结果, 参照图六, 施打UB-221的受试者中有60 %达到有效控制或治疗完成的指标 (HAS7≤6)及80 %达到有效控制的指标 (HAS7≤3), 且UB-221在相同剂量之下的complete hive response rate结果优于参考药ligelizumab。
总结对比与目前上市的抗IgE药物Xolair® (omalizumab), UB-221在试验中观察比Xolair®在施打第一针三周后才起效, UB-221起效更快且能中和更多血清中游离的IgE, 更能有效地缓解症状; 另外Xolair®在终止用药后会快速反弹上升, 而UB-221能够较长时间抑制IgE生成, 即便终止用药后, 也能减缓IgE反弹的速度。综合以上, UB-221在治疗IgE引起的过敏性疾病, 如慢性自发性荨麻疹及哮喘, 比Xolair®更具优势。
根据世界卫生组织 (WHO)数据显示, 过去几十年来工业化国家内患有过敏相关疾病的人数逐年攀升及患病年龄层逐年下降, 尤其40至50 %的学龄儿童至少对一种过敏原会产生过敏反应; 全世界约有15至20 %的人患有荨麻疹。定义每次至少一周复发两次且复发长达六周以上称之为慢性荨麻疹, 上述病患比例中约有30 %会长期复发, 约11至14 %的病患会长达五年以上的长期复发。评估全球过敏性药物市场, 其中慢性自发性荨麻疹治疗药物市场规模自2017年 (约8.63亿美元)至2022年 (约13.99亿美元)的年复合增长率为10.15 %; 其中气喘市场自2019年 (约180亿美元)至2027年 (预估260亿美元)的年复合增长率预估为4.5 %。已上市的抗IgE治疗性单抗药物Xolair®于2019年的全球总销售额是33亿美元, 根据上述UB-221前临床试验及一期临床试验数据所进行竟品分析 (见章节 2.2), UB-221相比于Xolair®, UB-221显示具有起效更快, 更有效缓解症状及更长效的优势, 因此UB-221应用于哮喘及荨麻疹的抗IgE治疗药物方面更具有竞争优势。此外, 基于UB-221作用机制涵盖抑制IgE合成, 故其适用范围估计比Xolair®更大。随着工业化发展及生活环境趋于复杂, 过敏性疾病问题持续增加及严重, 从慢性自发性荨麻疹及气喘等过敏性疾病的研究及相关临床数据来看, IgE依旧是最能广泛适用的靶点, 而UB-221则是目前同类型产品中极具优势及竞争力的治疗性单抗药物。